-
随着新型冠状病毒肺炎疫情的爆发与蔓延[1-3],2020年1月20日,国家卫生健康委员会发布公告,将新型冠状病毒肺炎纳入《中华人民共和国传染病防治法》规定的乙类传染病,并采取甲类传染病的预防、控制措施。世界卫生组织2020年2月11日将该病正式命名为Coronavirus Disease 2019(COVID-19)[4]。截至2020年3月17日,全国已累计报告确诊病例81 135例(含港澳台251例)[5],全球其他国家和地区累计报告确诊病例97 976例[6]。早期研究与分析表明,新型冠状病毒肺炎的基本再生数(R0)[7]所属区间约为[2.5, 4.0],如:2.47~2.86[1],1.4~3.9[8]和2.8~3.3[9],属于中-高等级传播能力的传染性疾病。文献[10]用指数增长法、最大似然法和SEIR模型分别对R0进行了估计,其估计区间分别为3.63~3.87,2.90~3.43和3.71~4.11。文献[11]系统介绍了COVID-19的病原学、流行病学、传播动力学、临床特征、治疗及防控等多个领域的最新研究进展,同时比较了COVID-19与SARS、中东呼吸综合症冠状病毒及H1N1流感病毒所致疫情特征的异同,为COVID-19的防控提供了决策依据。
随着防控措施的实施,传染病传播不再是自由传播阶段,为了评价防控措施的有效性,通常采用有效再生数对传染病的传播能力进行实时评估。有效再生数Rt定义为在某时刻t,一个感染者平均而言可以感染其他个体的数量[12]。如果知道传染病的传染链路,即知道谁将疾病传给了谁,那么有效再生数的计算只需要简单地统计每一个染病个体感染的下一代个体数量,最后取一个平均值即可得到有效再生数。但实际情况非常复杂,很难知道传染病的传染链路。针对这一问题,研究者设计了各种方法对不同场景和阶段下的有效再生数进行估计[13-18],进而对疫情发展态势进行预测和控制效果的评估。文献[13]提出了一种基于似然分析的有效再生数估计方法,被称为Willinga-Teunis方法。此方法只需要知道症状出现时间即可对传染病的有效再生数进行估计。该方法计算Rt时,需要知道t之后一个完整传播代际中被t时候出现症状的患者感染的总人数,而COVID-19代际时间(generation time,又称生成时间)的95%置信区间上界为19天[8],这就意味着这种方法有19天的延迟(本文取最大代际时间为21天),实时性得不到保障。针对这种情况,文献[14]对Willinga-Teunis方法[13]所得结果进行修正,从而使得即便没有达到一个最长代际时间,也可以较为准确地估计有效再生数。文献[18]基于COVID-19疫情网络公开数据,对全国、各省份以及武汉市不同时间基本再生数(R0)的动态变化R0(t)进行了估计,以评估在现有防控措施下,COVID-19传染速率随时间变化的趋势。分析表明,在疫情初期,全国整体R0(t)不稳定,数值较大,1月下旬开始呈现下降趋势,到2月初,下降趋势稳定。文献[19]利用病毒演化动力学方程,对易感再生数、当日感染概率、潜伏感染概率随时间的变化进行了分析,并利用时变参数对疫情发展进行了预测,结果表明在2020年2月9日左右,疫情发展会达到高峰,随后确诊人数将出现下降。
现有的方法,如Willinga-Teunis方法[13]、Cauchemez方法[14],都假设每个患者的症状出现时间是已知的,而通常情况下,很难获得所有患者的症状出现时间。本文利用已搜集到的少量包含症状出现时间的患者数据,提出了一种症状出现时间估计的有效方法,进而分析COVID-19的有效再生数,并对中国内地29个省、直辖市和自治区(青海、西藏数据太少,不具统计意义,没有进行分析)的防控效果进行评价。结果表明,在2020年1月20日实施甲级防控的两周内,COVID-19在所有省、直辖市和自治区都得到了有效的遏制(Rt<1),截至2020年2月21日,全国近7日的平均再生数已低至0.18,防控效果非常显著。
HTML
-
为了对有效再生数进行估计,除了需要知道患者的症状出现时间外,还需要知道此传染病的代际时间,定义为患者的症状出现时间与其下一代患者的症状出现时间的时间间隔。对代际时间的估计,通常根据早期临床诊断病例及接触情况,进行分析得到。文献[8]通过对武汉早期的425例患者进行实证分析,得到COVID-19代际时间tg的均值为7.5天,标准差为3.4天,近似服从形状参数
$\alpha = 4.866$ ,逆尺度参数$\,\beta = 0.649$ 的伽玛分布[20]:式中,
$\Gamma \left( \alpha \right)$ 是参数为$\alpha $ 的伽玛函数;形状参数$\alpha $ 和逆尺度参数$\,\beta $ 与伽玛分布的均值$\mu $ 和标准差$\sigma $ 存在如下简单关系,可用于计算$\alpha $ 和$\beta $ :假设要计算t时刻(单位:天)的有效再生数,就是要计算t时刻染病的人平均感染了多少人。考虑染病个体u,其感染时间tu=t,需要考察t时刻之后
$t_g^{\max }$ 天内($t_g^{\max }$ 为最长代际时间,实际计算时取$t_g^{\max } = 21$ [8])被感染的个体有多大概率是被患者u感染的。本文考虑u之后感染的某个个体v,其发病时间为tv(tu<tv)。现在以v为中心,考察tv之前$t_g^{\max }$ 内发病的个体,这些个体中每个个体w(u也包括在内)都可能感染v,感染的概率正比于$\tau ({t_v} - {t_w})$ ,因此,患者u导致患者v感染的概率可以估计为:根据式(3),可以得到:
对患者u,他导致tu+1到
${t_u} + t_g^{\max }$ 之间的患者v被感染的概率为pvu,由此,患者u感染的个体总数的期望可以近似为:对时刻t染病的每一个患者都可以算出这样一个期望值,因此,时刻t的有效再生数可以近似为:
式中,Ct是所有在时刻t出现症状的患者集合。假设每一个患者的传染能力和传染机会都均等的话,那么时刻t的有效再生数Rt和这一天的任一染病个体u感染的个体总数期望是相等的,即:
${R_t} = {E_u}(t = {t_u})$ 。进一步地,假设我们观察的时间窗口是[0,T],对第t天出现症状的患者,如果
$t + t_g^{\max } \leqslant T$ ,那么用Willinga-Teunis方法[13]对有效再生数${R_t}$ 进行估计完全可行。但如果$t + t_g^{\max } > T$ ,那么第t天出现症状的患者在T之后还可能感染新的个体,用Willinga-Teunis方法[13]估计得到的${R_t}$ 偏小,这时,需要对${R_t}$ 进行修正。如果将${R_t}$ 表示为:式中,
$R_t^ - $ 和$R_t^ + $ 分别表示第t天的个体在T及T之前和T之后平均感染的个体数量,$R_t^ - $ 可以用Willinga-Teunis方法[13]直接进行估计,再利用$R_t^ - $ 和tg分布对${R_t}$ 进行修正得到:不管是Willinga-Teunis方法[13]还是Cauchemez修正方法[14],都假设每个患者的症状出现时间是已知的。但实际上,很难获得所有患者的症状出现时间。为了对
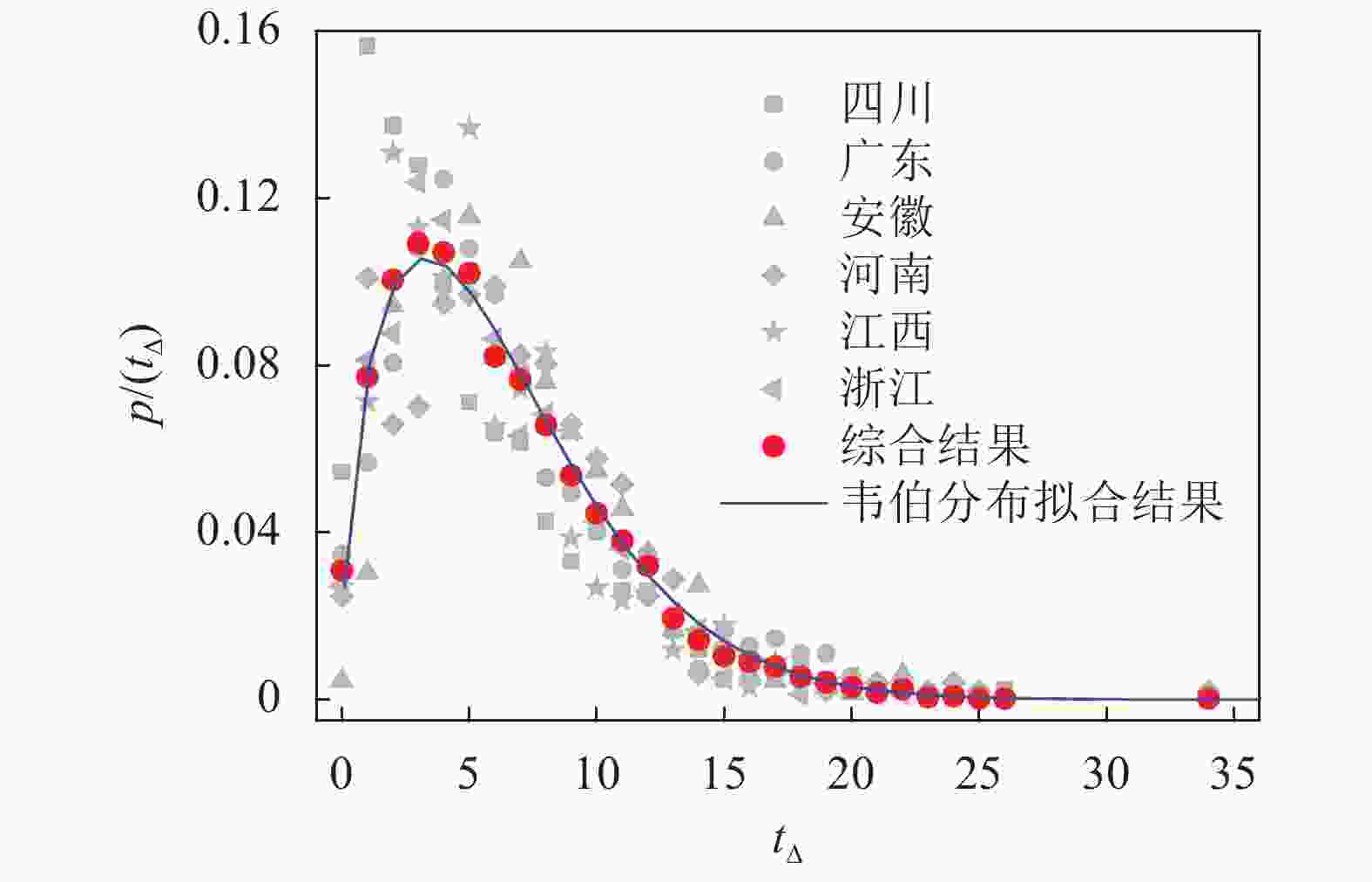
${R_t}$ 进行估计,需要对患者的症状出现时间进行估计。本文利用部分患者的症状出现时间和确诊时间,提出了一个估计所有患者症状出现时间的方法。根据已搜集到的包含症状出现时间和确诊时间的少量患者数据,首先对症状出现时间和确诊时间的间隔${t_\Delta }$ 进行实证分析,本文分析了四川、广东、安徽、河南、江西和浙江6省的间隔时间分布,如图1中灰色点所示,在6省结果基础上,进行简单算术平均得到了一个综合的间隔时间分布结果,如图1中红色实心点所示。实证分析得到的综合间隔时间可以用一个3参数(位置参数,形状参数和尺度参数)的韦伯分布[21]进行拟合,其密度函数为:式中,位置参数
$\gamma = 0.1$ ,形状参数$\alpha = 1.48$ ,尺度参数$\beta = 7.03$ ,如图1的实线所示。这里引入位置参数的原因在于:在实证分析结果中,有部分患者的症状出现时间和确诊时间在同一天,即$p({t_\Delta } = 0) > 0$ ,而对于标准的两参数韦伯分布$p({t_\Delta } = 0) = 0$ 。从图1可以看出,估计得到的韦伯分布与实证分析得到的综合时间间隔分布拟合得非常好,而综合时间间隔分布也能比较好的表征单一省份的时间间隔分布。本文利用估计得到的韦伯分布,结合患者的确诊时间,可以对症状出现时间采用蒙特卡洛方法抽样估计,进而采用本文介绍的方法计算有效再生数
${R_t}$ 。
-
本文搜集了2020年1月11日—2020年2月22日所有中国内地的确诊病例数据,累计确诊病例数量为76 936例[5],其中,本文还通过各种新闻报道获得了少部分病例(约占总病例的4.74%,主要包括四川、广东、安徽、河南、江西和浙江6个省的部分城市,共计3 650例)的症状出现时间。所有数据覆盖了中国内地29个省、直辖市和自治区,由于青海和西藏的病例太少,不具统计意义,本文没有包含这部分数据。针对其他国家,本文搜集了韩国截至2020年3月8日的数据,累计确诊病例数量7 313例,其中225例包含了患者的症状出现时间。
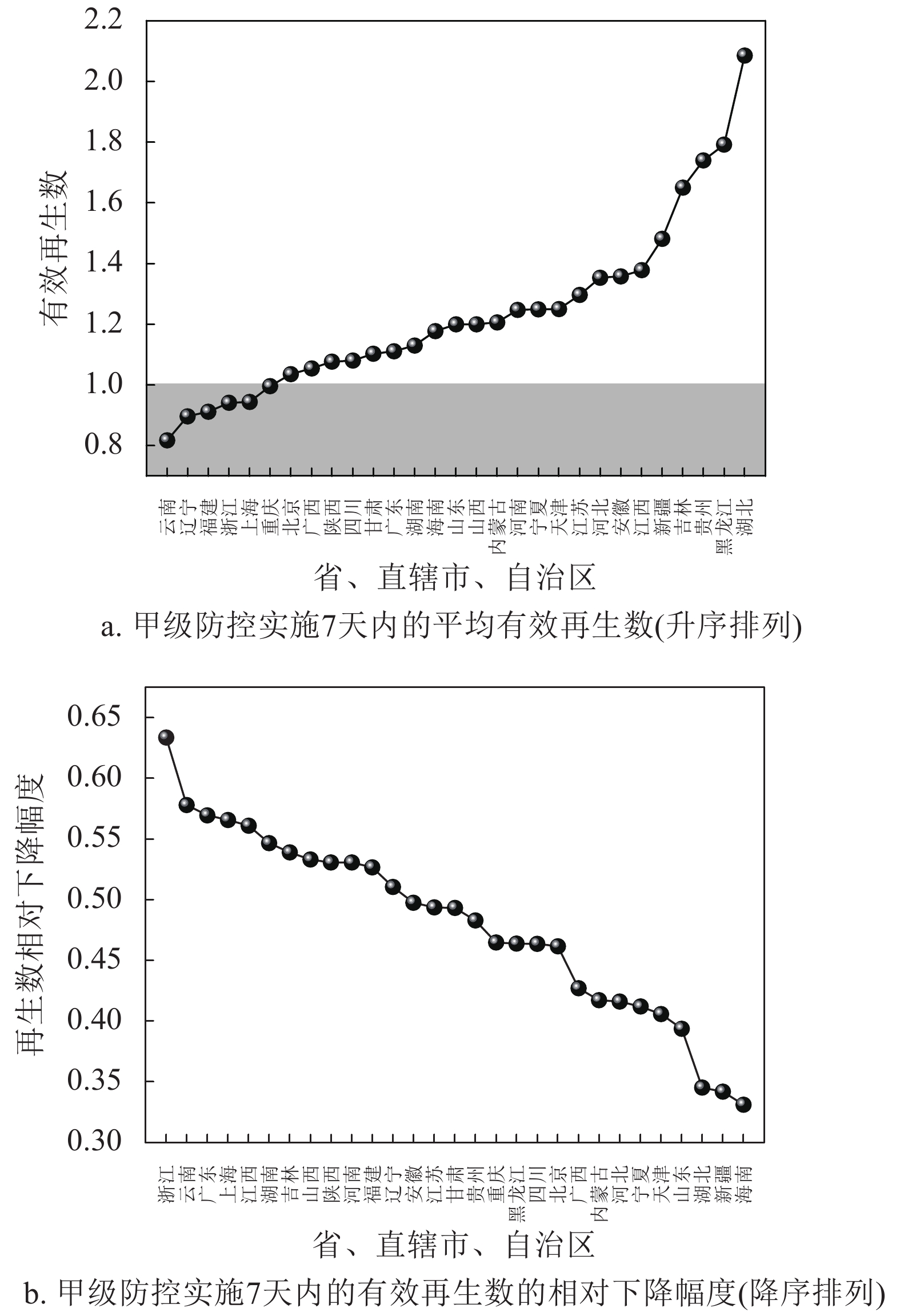
利用本文方法对中国内地除青海、西藏外的29个省、直辖市和自治区的有效再生数进行了估计。表1给出了截至2020年2月22日的累计确诊病例数、有效再生数Rt降至1以下的日期,表中的结果是10 000次独立实验的均值。如表1所示,在2020年1月20日全国出台COVID-19甲级防控措施后的两周内,全国所有省、直辖市和自治区的有效再生数都降到了1以下,大部分省甚至在一周之内就降到了1以下,有效遏制了COVID-19的蔓延和传播。表1还列出了截至2020年2月21日最近一周的平均有效再生数,几乎所有省的有效再生数都已经远小于1,全国的平均有效再生数已低至0.18。这些结果充分说明全国采取的防控策略极其有效,快速遏制住了疾病在全国的蔓延。
省、直辖市、
自治区累计确诊
病例数Rt降至1以
下的日期最近一周
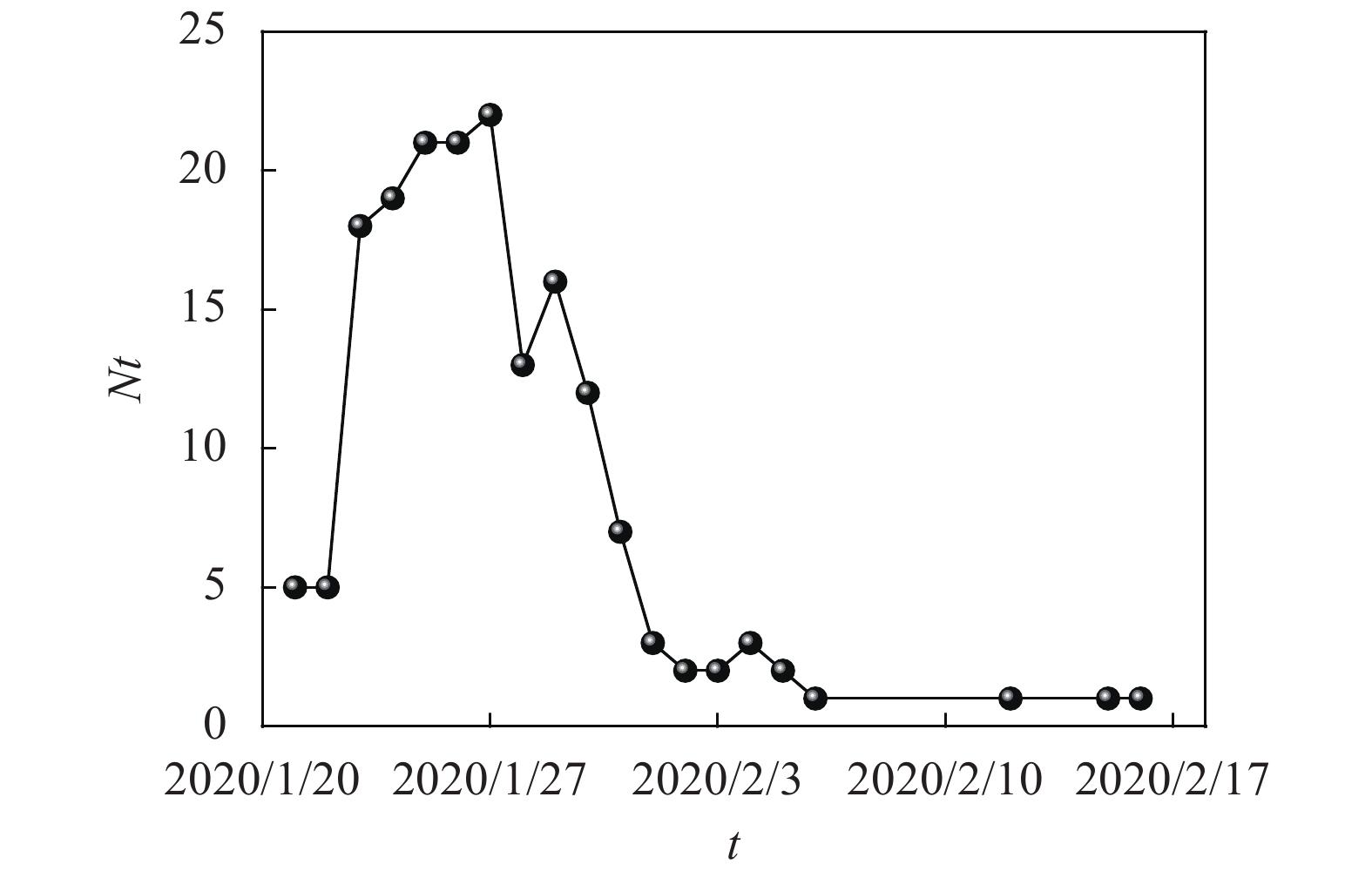
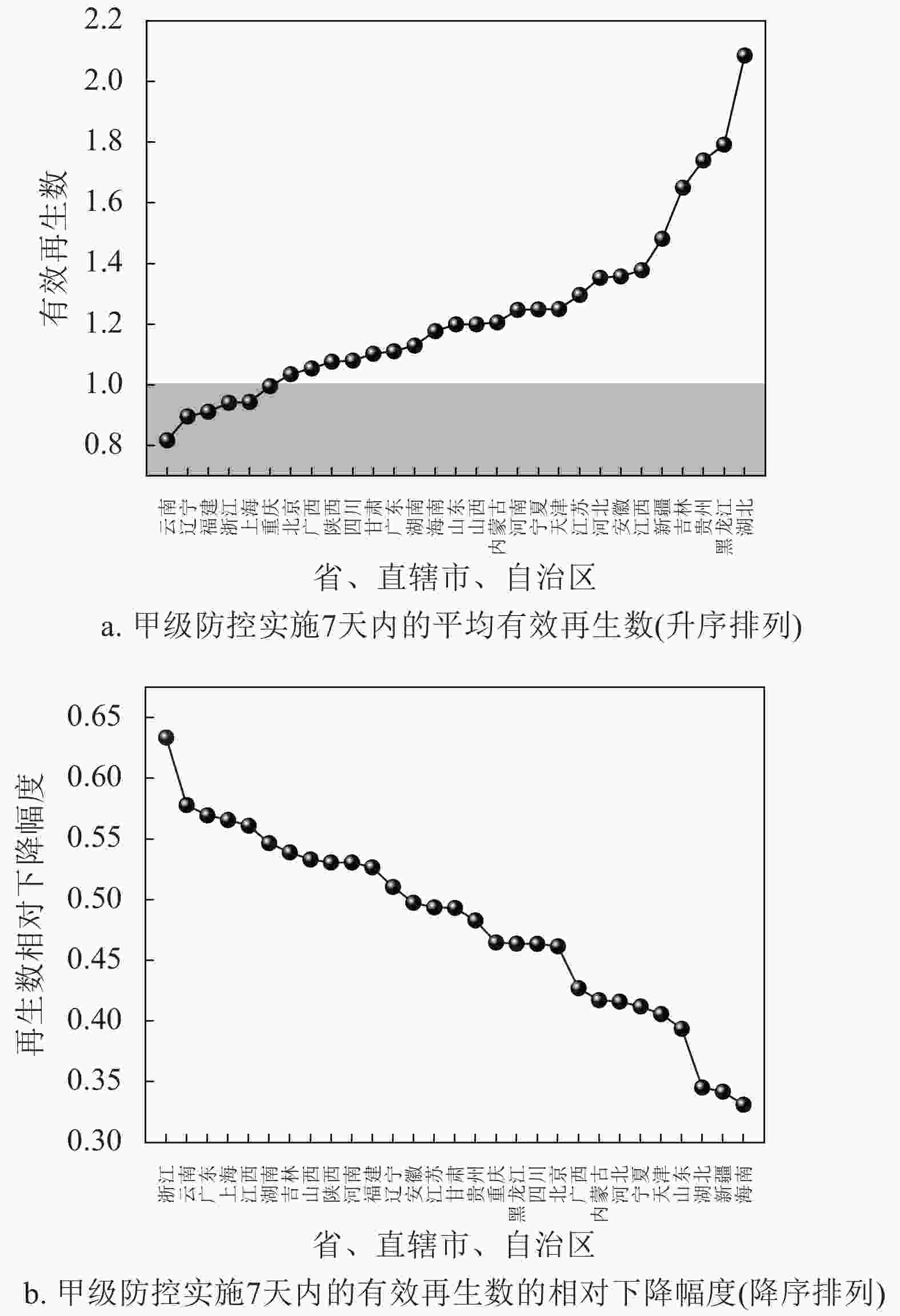
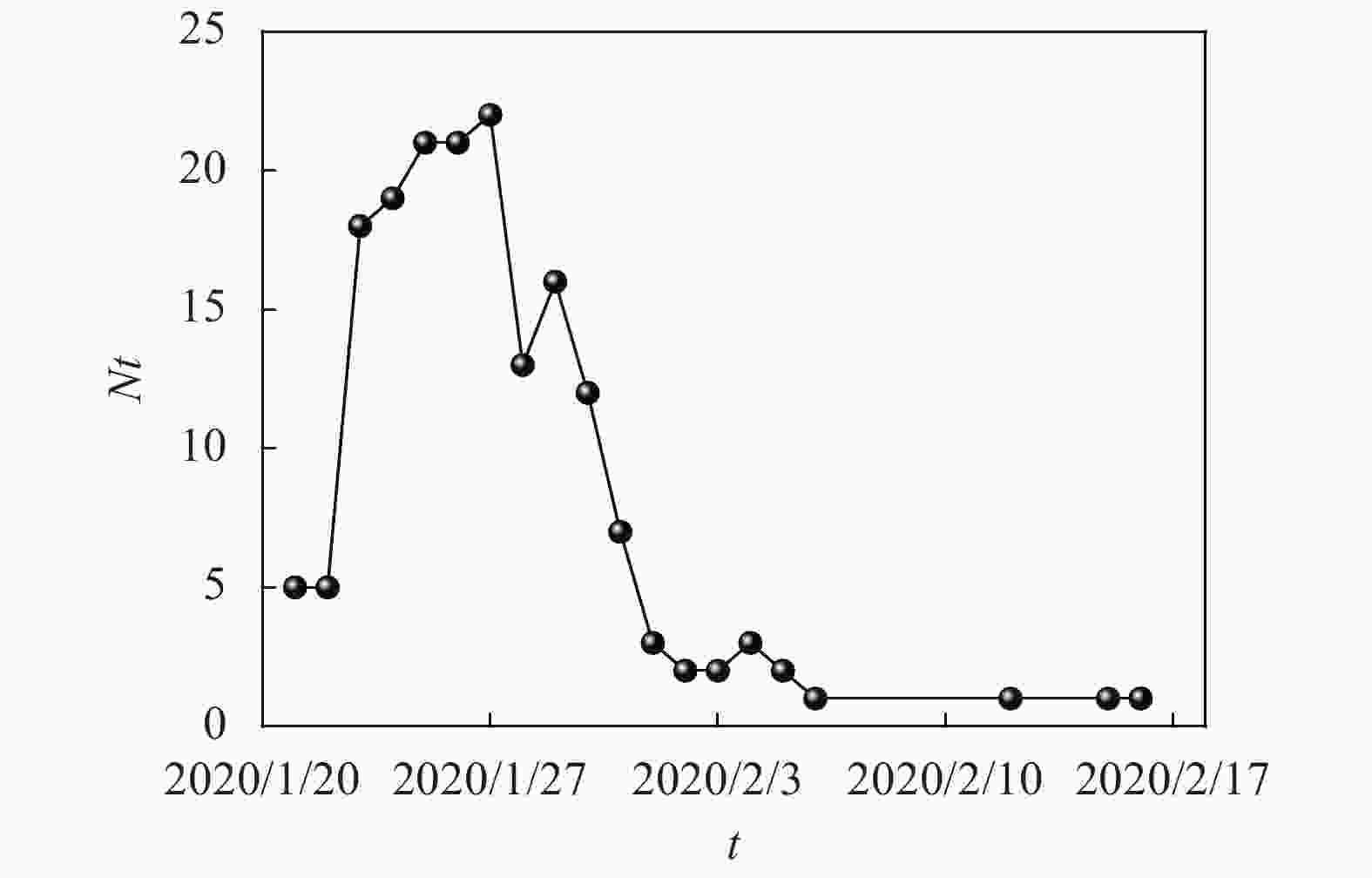
的平均Rt福建 298 2020/1/23 0.136 5 辽宁 121 2020/1/23 0.005 3 云南 174 2020/1/23 0.203 9 上海 335 2020/1/24 0.196 7 浙江 1 205 2020/1/24 0.289 5 重庆 573 2020/1/24 0.246 3 北京 399 2020/1/25 0.249 3 甘肃 91 2020/1/25 0.000 0 广东 1 342 2020/1/25 0.108 8 广西 249 2020/1/25 0.323 2 湖南 1 016 2020/1/25 0.132 1 陕西 245 2020/1/25 0.300 2 四川 526 2020/1/25 0.175 7 河南 1 271 2020/1/26 0.084 8 内蒙古 75 2020/1/26 0.317 6 宁夏 71 2020/1/26 0.014 6 山西 132 2020/1/26 0.278 0 山东 754 2020/1/27 0.497 7 安徽 989 2020/1/27 0.082 0 海南 168 2020/1/27 0.348 7 江苏 631 2020/1/27 0.090 1 江西 934 2020/1/27 0.055 6 天津 135 2020/1/27 0.424 1 河北 311 2020/1/28 0.173 6 吉林 91 2020/1/28 0.165 1 贵州 146 2020/1/29 0.015 6 黑龙江 480 2020/1/29 0.130 7 新疆 76 2020/1/30 0.132 0 湖北 64 287 2020/2/2 0.049 1 图2比较了中国内地29个省、直辖市、自治区在甲级防控后有效再生数一周内的变化情况。可以看出,实施甲级防控后,很多省市的新型冠状病毒肺炎迅速得到了遏制,甲级防控实施7天的相对降幅基本在40%以上。图3给出了各市防控情况的整体分析结果,其中横坐标是时间(天),纵坐标是在这个时间有效再生数降到1以下的城市数。只分析了累积确诊超过20例的城市。可以看出,在实施甲级防控7天内(2020年1月27日),就有超过60%的地级市的有效再生数降到了1以下,进一步说明了防控产生的显著效果。
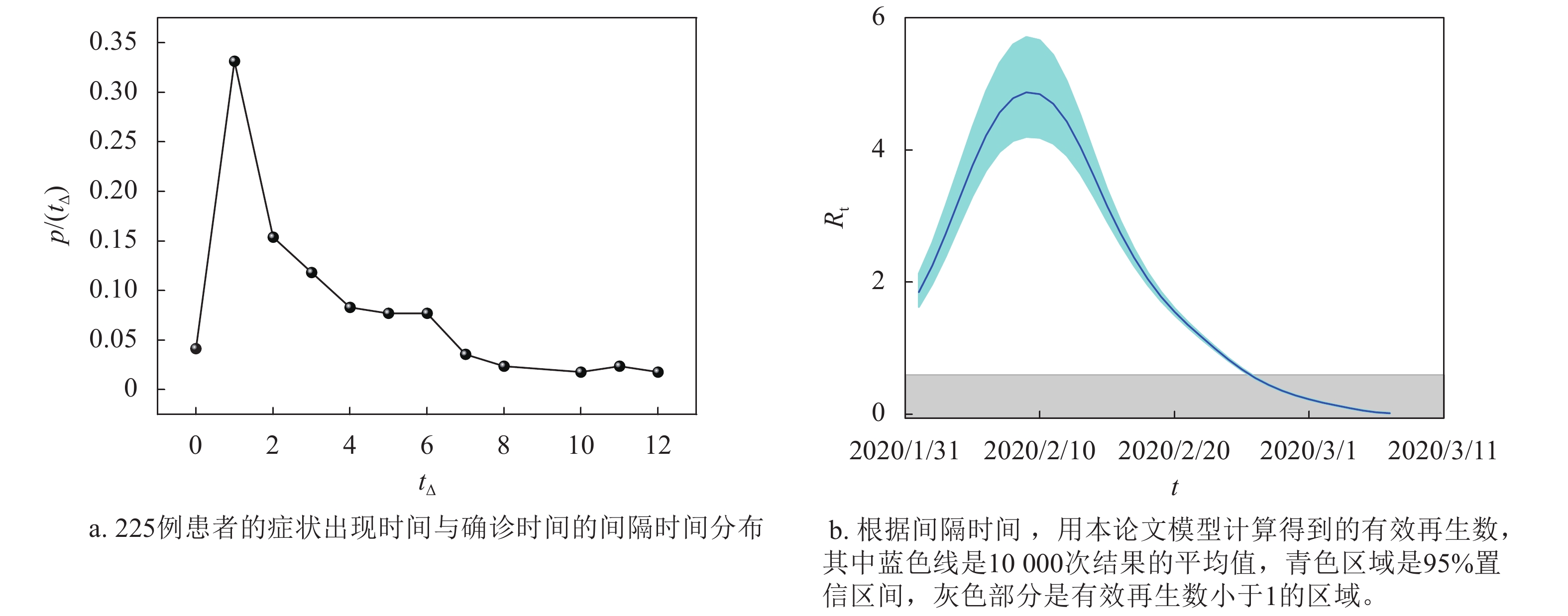
进一步利用本文提出的方法,对韩国的有效再生数进行了估计和分析,所用数据为截止2020年3月8日的确诊病例数。本文仍然假设COVID-19在韩国的代际时间为
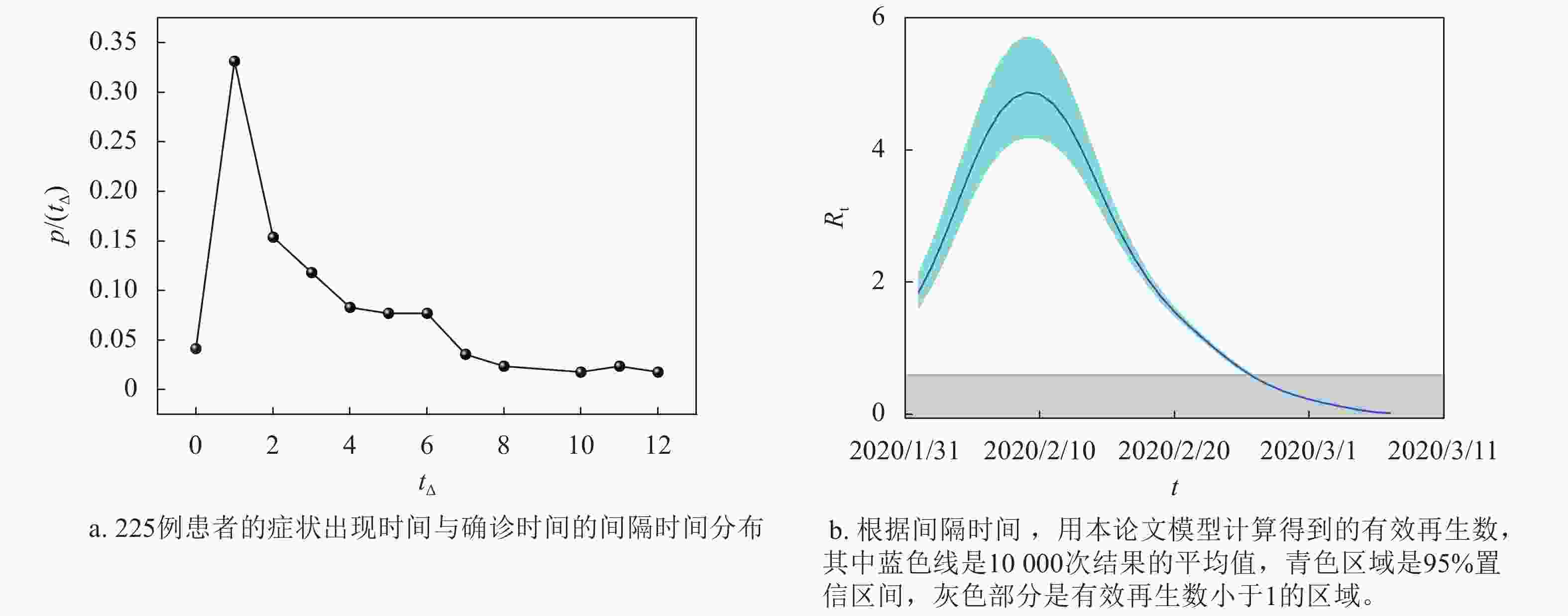
$7.5 \pm 3.4$ 天[8]。由于不同国家患者出现症状时间和确诊时间之间的间隔时间分布存在一定差异,在分析韩国的防控效果时,本文根据搜集到的韩国225名患者的出现症状时间和确诊时间构建了韩国的近似间隔时间分布,如图4a所示,整体上从出现症状到最后确诊的时间相对较短,间隔在2天以内的占到了41.5%。结合病例的确诊时间,对韩国的症状出现时间进行了估计,在此基础上进一步估计其有效再生数,如图4b所示。从图4的结果来看,韩国的有效再生数整体上呈现先升高再降低的态势,其最高有效再生数出现在2020年2月9号,其值一度超过5,随着防控措施的出台,有效再生数开始下降,在2020年2月25日降到了1以下,疾病传播得到了遏制。
-
本文根据新型冠状病毒肺炎患者的确诊时间及少部分患者的症状出现时间,构建了患者出现症状时间的反推计算模型,并利用蒙特卡洛方法,反推得到了患者的症状出现时间,结合文献[13-14]的研究成果,对中国各省市及其他国家防控措施的有效性进行了评价和分析。从分析结果来看,中国和韩国采取的防控措施在短时间内产生了显著的控制效果。本文方法仍然存在很多局限性,后续还有一系列问题值得进一步的探索和研究,主要包括:1) 本文假设症状出现时间与确诊时间的间隔分布保持不变,但实际上,随着对新型冠状病毒肺炎的认识,症状出现时间与确诊时间的间隔会越来越短,这使得在后期估计的症状出现时间比实际的症状出现时间要早,继而对有效再生数的估计也带来较大的偏差,对海外国家有效再生数的估计,由于包含症状出现时间的数据获取更少,造成有效再生数估计的偏差可能更大;2) 在估计有效再生数时,没有考虑输入病例的影响,这使得早期的有效再生数估计结果比实际结果偏大;3) 确诊病人入院后,基本上就截断了他的传播途径,这在本文的模型中也没有考虑,对有效再生数的计算造成一定的影响,后续可以考虑输入病例、入院病例和康复的影响进一步提升模型估计效果[22]。为更好地认识和遏制传染病的传播,建议各国在不泄露个人隐私的情况下,尽可能开放一些必要的数据,比如症状出现时间、入院时间、治愈/死亡时间等。

 ISSN
ISSN 











































 DownLoad:
DownLoad: